
|

|
Большая Советская Энциклопедия (цитаты)
|

|

|
 |
Фосфор | (далее Ф)(лат. Phosphorus), Р, элемент группы периодической системы номер 15, масса 30,97376, неметалл. Природный Ф состоит из одного стабильного изотопа 31; получено шесть искусственных радиоактивных изотопов: 28 (T1/2 = 6,27 сек), 29 (T1/2 = 4,45 сек); 30 (T1/2 = 2,55 мин), 31 (T1/2 = 14,22 сут), 32 (T1/2 = 25 сут), 33 (T1/2 = 12,5 сек). Наибольшее значение имеет 32, обладающий значительной энергией b-излучения и применяемый в и биохимических исследованиях в качестве меченого
Историческая справка. По некоторым литературным данным, способ получения Ф был известен еще араб. алхимикам 12 в. Но общепринятой датой открытия Ф считается 1669, когда Х. Бранд ( при прокаливании с песком сухого остатка от выпаривания мочи и последующей перегонкой без доступа воздуха получил светящееся в темноте вещество, названное сначала "холодным огнем", а позднее Ф от греч. phosphóros – светоносный. Вскоре способ получения Ф стал известен нем. химикам – И. Крафту, И. Кункелю; в 1682 об этом способе было опубликовано. В 1743 А. С. Маргграф разработал следующий способ получения Ф смесь с мочой выпаривалась досуха и нагревалась до прекращения выделения летучих продуктов; остаток смешивали с древесным углем в порошке и подвергали перегонке в глиняной реторте; пары Ф конденсировались в приемнике с водой. Наиболее простой метод получения Ф прокаливанием костяной золы с углем был предложен лишь в 1771 К. Шееле. Элементарную природу Ф установил А. Лавуазье. Во 2-й половине 19 в. возникло промышленное производство Ф из в ретортных печах; в начале 20 в. они были заменены электрическими печами.
Распространение в природе. Среднее содержание Ф в земной коре (кларк) – 9,3×10-2% по массе; в средних горных породах 1,6×10-1, в основных породах 1,4×10-1, меньше в гранитах и др. кислых изверженных породах – 7×10-2 и еще меньше в ультраосновных породах (мантии) – 1,7×10-2%; в осадочных горных породах от 1,7×10-2 (песчаники) до 4×10-2% (карбонатные породы). Ф принимает участие в магматических процессах и энергично мигрирует в биосфере. С обоими процессами связаны его крупные накопления, образующие промышленные месторождения апатитов и фосфоритов (см. Фосфатные руды). Ф – исключительно важный биогенный элемент, он накапливается многими организмами. С биогенной миграцией связаны многие процессы концентрации Ф в земной коре. Из вод Ф легко осаждается в виде нерастворимых минералов или захватывается живым веществом. Поэтому в морской воде лишь 7×10-6% Ф Известно около 180 минералов Ф в основном – это различные фосфаты, из которых наиболее распространены фосфаты (см. Фосфаты природные).
Физические свойства. Элементарный Ф существует в виде нескольких аллотропических модификаций, главная из которых – белая, красная и черная. Белый Ф – воскообразное, прозрачное вещество с характерным запахом, образуется при конденсации паров Ф Белый Ф в присутствии примесей – следов красного Ф и т.п. – окрашен в желтый цвет, поэтому товарный белый Ф называется желтым. Существуют две формы белого Ф a- и b-форма. a-модификация представляет собой кубической системы (а = 18,5 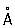 ); плотность 1,828 г/см3, tпл 44,1 °С, tкип 280,5 °, теплота плавления 2,5 кдж/моль 4 (0,6 ккал/моль 4), теплота испарения 58,6 кдж/моль Р4(14,0 ккал/моль 4), давление пара при 25 °С 5,7 н/м2 (0,043 мм рт. ст.). Коэффициент линейного расширения в интервале температур от 0 до 44 °С равен 12,4×10-4, теплопроводность 0,56 вт/(м×К) (1,1346×10-3 кал/(см×сек×°С)) при 25 °С. По электрическим свойствам "белый Ф близок к диэлектрикам: ширина запрещенной зоны около 2,1 эв, удельное электросопротивление 1,54×1011 ом×см, диамагнитен, удельная восприимчивость – 0,86×10-6. Твердость по Бринеллю 6 Мн/м2 (0,6 кгс/мм2). a-форма белого Ф хорошо растворяется в сероуглероде, хуже – в жидком аммиаке, бензоле, четыреххлористом и др. При – 76,9 °С и давлении 0,1 Мн/м2 (1 кгс/см2) a-форма переходит в низкотемпературную b-форму (плотность 1,88 г/см3). С повышением давления до 1200 Мн/м2 (12 тыс. кгс/см2) переход происходит при 64,5 °С. b-форма – с двойным лучепреломлением, их структура окончательно не установлена. Белый Ф ядовит: на воздухе при температуре около 40 °С самовоспламеняется, поэтому его следует хранить под водой (растворимость в воде при 25 °С 3,3×10-4%). Нагреванием белого Ф без доступа воздуха при 250–300 °С в течение нескольких часов получают красный Ф Переход экзотермичен, ускоряется ультрафиолетовыми лучами, а также примесями (иод, Обычный товарный красный Ф практически полностью аморфен; имеет цвет от темно-коричневого до фиолетового. При длительном нагревании, необратимо может переходить в одну из форм (триклинную, кубическую и др.) с различными свойствами: плотностью от 2,0 до 2,4 г/см3, tпл от 585 до 610 °С при давлении в несколько десятков атмосфер, температурой возгонки от 416 до 423 °С, удельным электросопротивлением от 109 до 1014 ом×см. Красный Ф на воздухе не самовоспламеняется; вплоть до температуры 240–250 °С, но самовоспламеняется при трении или ударе; нерастворим в воде, а также в бензоле, сероуглероде и др., растворим в трибромиде Ф При температуре возгонки красный Ф превращается в пар, при охлаждении которого образуется в основном белый Ф ); плотность 1,828 г/см3, tпл 44,1 °С, tкип 280,5 °, теплота плавления 2,5 кдж/моль 4 (0,6 ккал/моль 4), теплота испарения 58,6 кдж/моль Р4(14,0 ккал/моль 4), давление пара при 25 °С 5,7 н/м2 (0,043 мм рт. ст.). Коэффициент линейного расширения в интервале температур от 0 до 44 °С равен 12,4×10-4, теплопроводность 0,56 вт/(м×К) (1,1346×10-3 кал/(см×сек×°С)) при 25 °С. По электрическим свойствам "белый Ф близок к диэлектрикам: ширина запрещенной зоны около 2,1 эв, удельное электросопротивление 1,54×1011 ом×см, диамагнитен, удельная восприимчивость – 0,86×10-6. Твердость по Бринеллю 6 Мн/м2 (0,6 кгс/мм2). a-форма белого Ф хорошо растворяется в сероуглероде, хуже – в жидком аммиаке, бензоле, четыреххлористом и др. При – 76,9 °С и давлении 0,1 Мн/м2 (1 кгс/см2) a-форма переходит в низкотемпературную b-форму (плотность 1,88 г/см3). С повышением давления до 1200 Мн/м2 (12 тыс. кгс/см2) переход происходит при 64,5 °С. b-форма – с двойным лучепреломлением, их структура окончательно не установлена. Белый Ф ядовит: на воздухе при температуре около 40 °С самовоспламеняется, поэтому его следует хранить под водой (растворимость в воде при 25 °С 3,3×10-4%). Нагреванием белого Ф без доступа воздуха при 250–300 °С в течение нескольких часов получают красный Ф Переход экзотермичен, ускоряется ультрафиолетовыми лучами, а также примесями (иод, Обычный товарный красный Ф практически полностью аморфен; имеет цвет от темно-коричневого до фиолетового. При длительном нагревании, необратимо может переходить в одну из форм (триклинную, кубическую и др.) с различными свойствами: плотностью от 2,0 до 2,4 г/см3, tпл от 585 до 610 °С при давлении в несколько десятков атмосфер, температурой возгонки от 416 до 423 °С, удельным электросопротивлением от 109 до 1014 ом×см. Красный Ф на воздухе не самовоспламеняется; вплоть до температуры 240–250 °С, но самовоспламеняется при трении или ударе; нерастворим в воде, а также в бензоле, сероуглероде и др., растворим в трибромиде Ф При температуре возгонки красный Ф превращается в пар, при охлаждении которого образуется в основном белый Ф
При нагревании белого Ф до 200–220 °С под давлением (1,2–1,7)×103Мн/м2 ((12–17)×103 кгс/см2) образуется черный Ф Это превращение можно осуществить без давления, но в присутствии и небольшого количества черного Ф (затравки) при 370 °С в течение 8 сут. Черный Ф представляет собой ромбической структуры (а = 3,31 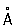 , b = 4,38 , b = 4,38 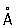 , с = 10,50 , с = 10,50 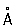 ), решетка построена из волокнистых слоев с характерным для Ф пирамидальным расположением плотность 2,69 г/см3, tпл около 1000 °С под давлением 1,8×103 Мн/м2 (18×103 кгс/см2). По внешнему виду черный Ф похож на графит; полупроводник: ширина запрещенной зоны 0,33 эв при 25 °С; имеет удельное электросопротивление 1,5 ом×см, температурный коэффициент электросопротивления 0,0077, диамагнитен, удельная восприимчивость – 0,27×10-6. При нагревании до 560–580 °С под давлением собственных паров превращается в красный Ф Черный Ф малоактивен, с трудом воспламеняется при поджигании, поэтому его можно безопасно подвергать механической обработке на воздухе. ), решетка построена из волокнистых слоев с характерным для Ф пирамидальным расположением плотность 2,69 г/см3, tпл около 1000 °С под давлением 1,8×103 Мн/м2 (18×103 кгс/см2). По внешнему виду черный Ф похож на графит; полупроводник: ширина запрещенной зоны 0,33 эв при 25 °С; имеет удельное электросопротивление 1,5 ом×см, температурный коэффициент электросопротивления 0,0077, диамагнитен, удельная восприимчивость – 0,27×10-6. При нагревании до 560–580 °С под давлением собственных паров превращается в красный Ф Черный Ф малоактивен, с трудом воспламеняется при поджигании, поэтому его можно безопасно подвергать механической обработке на воздухе.
радиус Ф 1,34 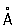 , ионные радиусы: 5 + 0,35 , ионные радиусы: 5 + 0,35 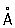 , 3 + 0,44 , 3 + 0,44 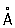 , 3- 1,86 , 3- 1,86 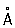 . .
Ф объединяются в двухатомные (2), четырехатомные (4) и полимерные молекулы. Наиболее стабильны при нормальных условиях полимерные молекулы, содержащие длинные цепи связанных между собой 4 – тетраэдров. В жидком, твердом виде (белый Ф и в парах ниже 800 °С Ф состоит из молекул 4. При температурах выше 800 °С молекулы 4 диссоциируют на 2, которые, в свою очередь, распадаются на при температуре свыше 2000 °С. Только белый Ф состоит из молекул 4, все остальные модификации – полимеры.
свойства. Конфигурация внешних электронов Ф 3s23p3, в соединениях наиболее характерны степени окисления + 5, + 3, и – 3. Подобно Ф в соединениях главным образом ковалентен. Ионных соединений, подобных фосфидам 3, 32, очень мало. В отличие от Ф обладает свободными 3d-opбиталями с довольно низкими энергиями, что приводит к возможности увеличения координационного числа и образованию донорно-акцепторных связей.
Ф активен, наибольшей активностью обладает белый Ф красный и черный Ф в реакциях гораздо пассивнее. Окисление белого Ф происходит по механизму цепных реакций. Окисление Ф обычно сопровождается хемилюминесценцией. При горении Ф в избытке образуется пятиокись 410 (или 25), при недостатке – в основном трехокись 46 (или 23). Спектроскопически доказано существование в парах 47, 48, 26, и др. фосфора окислов. Пятиокись Ф получают в промышленных масштабах сжиганием элементарного Ф в избытке сухого воздуха. Последующая гидратация 410 приводит к получению орто- (Н3РО4) и поли- (Нn + 2n3п + 1) кислот. Кроме того, Ф образует фосфористую кислоту 33, фосфорноватую кислоту 426 и фосфорноватистую кислоту 32, а также надкислоты: надфосфорную 428 и мононадфосфорную 35 Широкое применение находят соли кислот (фосфаты), в меньшей степени – фосфиты и гипофосфиты.
Ф непосредственно соединяется со всеми галогенами с выделением большого количества тепла и образованием тригалогенидов (PX3, где Х – галоген), пентагалогенидов (PX5) и оксигалогенидов (например, POX3) (см. Фосфора галогениды). При сплавлении Ф с серой ниже 100 °С образуются твердые растворы на основе Ф и серы, а выше 100 °С происходит экзотермическая реакция образования сульфидов 43, 45, 47, 410, из которых только 45 при нагревании выше 200 °С разлагается на 43 и 47, а остальные плавятся без разложения. Известны оксисульфиды 232, 233, 443, 6105 и 443. Ф по сравнению с менее способен к образованию соединений с фосфин 3 и дифосфин 24 могут быть получены только косвенным путем. Из соединений Ф с известны нитриды , 23, 35 – твердые, устойчивые вещества, полученные при пропускании с парами Ф через электрическую дугу; полимерные фосфонитрилгалогениды – (PNX2) n (например, полифосфонитрилхлорид), полученные взаимодействием пентагалогенидов с аммиаком при различных условиях; амидоимидофосфаты – соединения, как правило, полимерные, содержащие наряду с Р–О–Р связями Р––Р связи.
При температурах выше 2000° Ф реагирует с с образованием карбида 3 – вещества, не растворяющегося в обычных растворителях и не взаимодействующего ни с кислотами, ни со щелочами. При нагревании с металлами Ф образует фосфиды.
Ф образует многочисленные фосфорорганические соединения.
Получение. производство элементарного Ф осуществляется электротермическим восстановлением его из природных фосфатов (апатитов или при 1400–1600 °С коксом в присутствии кремнезема (кварцевого песка):
23(4)2 + 10 + n2 = 4 + 10 + 6×n2
Предварительно измельченная и обогащенная руда смешивается в заданных соотношениях с кремнеземом и коксом и загружается в электропечь. Кремнезем необходим для снижения температуры реакции, а также увеличения ее скорости за счет связывания выделяющейся в процессе восстановления окиси в силикат который непрерывно удаляется в виде расплавленного шлака. В шлак переходят также силикаты и окислы и др. примеси, а также феррофосфор (2, , 3), образующийся при взаимодействии части восстановленного с Ф Феррофосфор, а также растворенные в нем небольшие количества фосфидов и др. металлов по мере накопления удаляются из электропечи с целью последующего использования при производстве специальных сталей.
Пары Ф выходят из электропечи вместе с газообразными побочными продуктами и летучими примесями (, 4, 3, пары воды, продукты пиролиза органических примесей шихты и др.) при температуре 250–350 °С. После очистки от пыли содержащие газы направляют в конденсационные установки, в которых при температуре не ниже 50 °С собирают под водой жидкий технический белый Ф
Разрабатываются методы получения Ф с применением газообразных восстановителей, плазменных реакторов с целью интенсификации производства за счет повышения температур до 2500–3000 °С, т. е. выше температур диссоциации природных фосфатов и газов-восстановителей (например, метана), используемых в качестве транспортирующего газа в низкотемпературной плазме.
Применение. Основная масса производимого Ф перерабатывается в фосфорную кислоту и получаемые на ее основе фосфорные удобрения и технические соли (фосфаты).
Белый Ф используется в зажигательных и дымовых снарядах, бомбах; красный Ф – в спичечном производстве. Ф применяется в производстве сплавов цветных металлов как раскислитель. Введение до 1% Ф увеличивает жаропрочность таких сплавов, как фехраль, Ф входит в состав некоторых бронз, т.к. повышает их жидкотекучесть и стойкость против истирания. Фосфиды металлов, а также некоторых неметаллов (В, , и т.п.) используются при получении и легировании полупроводниковых материалов. Частично Ф применяется для получения и сульфидов, которые служат исходными веществами для производства пластификаторов (например, трикрезилфосфат, трибутилфосфат и др.), медикаментов, фосфорорганических пестицидов, а также применяются в качестве добавок в смазочные вещества и в горючее.
Техника безопасности. Белый Ф и его соединения высокотоксичны. Работа с Ф требует тщательной герметизации аппаратуры; хранить белый Ф следует под водой или в герметически закрытой металлической таре. При работе с Ф следует строго соблюдать правила техники безопасности.
Л. В. Кубасова.
Ф в организме. Ф – один из важнейших биогенных элементов, необходимый для жизнедеятельности всех организмов. Присутствует в живых клетках в виде орто- и пирофосфорной кислот и их производных, а также входит в состав нуклеотидов, нуклеиновых кислот, фосфопротеидов, фосфолипидов, эфиров углеводов, многих коферментов и др. органических соединений. Благодаря особенностям строения Ф подобно серы, способны к образованию богатых энергией связей в макроэргических соединениях; кислоте (АТФ), креатин фосфате и др. (см. Окислительное фосфорилирование). В процессе биологической эволюции именно соединения стали основными, универсальными хранителями генетической информации и переносчиками энергии во всех живых системах. Др. важная роль соединений Ф в организме заключается в том, что ферментативное присоединение остатка (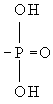 ) к различным органическим соединениям (фосфорилирование) служит как бы "пропуском" для их участия в обмене веществ, и, наоборот, отщепление остатка (дефосфорилирование) исключает эти соединения из активного обмена. Ферменты обмена Ф – киназы, фосфорилазы и фосфатазы. Главную роль в превращениях соединений Ф в организме животных и человека играет печень. Обмен соединений регулируется гормонами и витамином D. ) к различным органическим соединениям (фосфорилирование) служит как бы "пропуском" для их участия в обмене веществ, и, наоборот, отщепление остатка (дефосфорилирование) исключает эти соединения из активного обмена. Ферменты обмена Ф – киназы, фосфорилазы и фосфатазы. Главную роль в превращениях соединений Ф в организме животных и человека играет печень. Обмен соединений регулируется гормонами и витамином D.
Содержание Ф (в мг на 100 г сухого вещества) в тканях растений – 230–350, морских животных – 400–1800, наземных – 1700–4400, у бактерий – около 3000; в организме человека особенно много Ф в костной ткани (несколько более 5000), в тканях мозга (около 4000) и в мышцах (220–270). Суточная потребность человека в Ф 1–1,2 г (у детей она выше, чем у взрослых). Из продуктов питания наиболее богаты Ф сыр, мясо, яйца, зерно бобовых культур (горох, фасоль и др.). Баланс Ф в организме зависит от общего состояния обмена веществ. Нарушение обмена приводит к глубоким биохимическим изменениям, в первую очередь в энергетическом обмене. При недостатке Ф в организме у животных и человека развиваются остеопороз и др. заболевания костей, у растений – голодание (см. Диагностика питания растений). Источником Ф в живой природе служат его неорганические соединения, содержащиеся в почве и растворенные в воде. Из почвы Ф извлекается растениями в виде растворимых фосфатов. Животные обычно получают достаточное количество Ф с пищей. После гибели организмов Ф вновь поступает в почву и донные отложения, участвуя т. о. в круговороте веществ. Важная роль Ф в регуляции обменных процессов обусловливает высокую чувствительность многих ферментных систем живых клеток к действию соединений. Это обстоятельство используют в медицине при разработке лечебных препаратов, в сельском хозяйстве при производстве фосфорных удобрений, а также при создании эффективных инсектицидов. Многие соединения Ф чрезвычайно токсичны и некоторые из соединений могут быть причислены к боевым отравляющим веществам (зарин, зоман, табун). Радиоактивный изотоп Ф 32 широко используют в биологии и медицине как индикатор при исследовании всех видов обмена веществ и энергии в живых организмах (см. Изотопные индикаторы).
Н. Н. Чернов.
Отравления Ф и его соединениями наблюдаются при их термоэлектрической возгонке, работе с белым Ф производстве и применении соединений. Высокотоксичны фосфорорганические соединения, оказывающие антихолинэстеразное действие. Ф проникает в организм через органы дыхания, желудочно-кишечный тракт, кожу. Острые отравления проявляются жжением во рту и желудке, головной болью, слабостью, тошнотой, рвотой. Через 2–3 сут возникают боли в подложечной области, правом подреберье, желтуха. Для хронических отравлений характерны воспаление слизистых оболочек верхних дыхательных путей, признаки токсического гепатита, нарушение обмена (развитие остеопороза, ломкость, иногда омертвение костной ткани, чаще – на нижней челюсти), поражение сердечно-сосудистой и нервной систем. Первая помощь при остром отравлении через рот (наиболее частом) – промывание желудка, слабительное, очистительные клизмы, внутривенно растворы и др. При ожогах кожи – обработать пораженные участки растворами купороса или соды. Глаза промывают 2%-ным раствором питьевой соды. Профилактика: соблюдение правил техники безопасности, личная гигиена, уход за полостью рта, раз в 6 мес – медицинские осмотры работающих с Ф
Лекарственные препараты, содержащие Ф ( кислота, фитин, глицерофосфат фосфрен и др.), влияют главным образом на процессы тканевого обмена и применяются при заболеваниях мышц, нервной системы, при туберкулезе, упадке питания, малокровии и др. Радиоактивные изотопы Ф используют в качестве изотопных индикаторов для изучения обмена веществ, диагностики заболеваний, а также для лучевой терапии опухолей (см. также Радиоактивные препараты).
А. А. Каспаров.
Лит.: Краткая энциклопедия, т. 5, М., 1967; Коттон Ф Уилкинсон Дж., Современная неорганическая пер. с англ., ч. 2, М., 1969; Везер Ван-Дж.. и его соединения, пер. с англ., т. 1, М., 1962; Ахметов Н. С., Неорганическая 2 изд., М., 1975; Некрасов Б. В., Основы общей химии, 3 изд., т. 1–2, М., 1973; Моссэ А. Л., Печковский В. В., Применение низкотемпературной плазмы в технологии неорганических веществ, Минск, 1973; Горизонты биохимии, Сб. ст., пер. с англ., М., 1964; Рапопорт С. М., Медицинская биохимия, пер, с нем., М., 1966; Скулачев В. П., Аккумуляция энергии в клетке, М., 1969; Происхождение жизни и эволюционная биохимия, М., 1975.
|
Для поиска, наберите искомое слово (или его часть) в поле поиска
|

|
 |
 |
 |
|