
|

|
Большая Советская Энциклопедия (цитаты)
|

|

|
 |
Кельвина уравнение | Кельвина уравнение (далее К)характеризует изменение давления пара жидкости или растворимости твердых тел, вызванное искривлением поверхности раздела смежных фаз (поверхности соприкосновения твердого тела с жидкостью или жидкости с паром). Так над сферическими каплями жидкости давление насыщенного пара р повышено по сравнению с его давлением po над плоской поверхностью при той же температуре Т. Соответственно, растворимость с твердого вещества с выпуклой поверхностью выше, чем растворимость с0 плоских поверхностей того же вещества. Кельвина уравнение получено У. Томсоном (Кельвином) в 1871 из условия равенства химических потенциалов в смежных фазах, находящихся в состоянии термодинамического равновесия, и имеет вид: 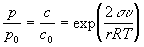 , где r — радиус средней кривизны поверхности раздела фаз, s — межфазное поверхностное натяжение, u — молярный объем жидкости или твердого тела, давление пара р или растворимость с которых фигурируют в уравнении, и R — газовая постоянная. Для шарообразных частиц r по абсолютной величине равен их радиусу. , где r — радиус средней кривизны поверхности раздела фаз, s — межфазное поверхностное натяжение, u — молярный объем жидкости или твердого тела, давление пара р или растворимость с которых фигурируют в уравнении, и R — газовая постоянная. Для шарообразных частиц r по абсолютной величине равен их радиусу.
Понижение или повышение давления пара и растворимости, в соответствии с Кельвина уравнение, зависит от знака кривизны поверхности рассматриваемого вещества; повышение отвечает выпуклой поверхности (r > 0), а понижение — вогнутой (r < 0). Так, в отличие от рассмотренных выше случаев, давление пара в пузырьке или над поверхностью вогнутого мениска в капилляре понижено (р < po). Т. к. значения р и с различны для частиц разных размеров или для участков поверхностей, имеющих впадины и выступы, Кельвина уравнение определяет направление переноса вещества (от больших значений р и с — к меньшим) в процессе перехода системы к состоянию термодинамического равновесия. Это приводит, в частности, к тому, что крупные капельки или частицы растут за счет испарения (растворения) более мелких, а неровные поверхности сглаживаются за счет растворения выступов и заполнения впадин. Заметные отличия давления и растворимости имеют место лишь при достаточно малых r. Поэтому Кельвина уравнение наиболее широко используется для характеристики состояния малых объектов (частиц коллоидных систем, зародышей новой фазы) и при изучении капиллярных явлений.
Н. В. Чураев. |
Для поиска, наберите искомое слово (или его часть) в поле поиска
|

|
 |
 |
 |

|

|
Новости 21.11.2024 11:29:48
|

|

|
 |
|

|
 |
 |
 |
|