
|

|
Большая Советская Энциклопедия (цитаты)
|

|

|
 |
Спирты | Спирты (далее С) производные углеводородов, содержащие в молекуле одну или несколько гидроксильных групп (—ОН) у насыщенных Соединения с ОН-группами в ароматическом кольце называются фенолами, с ОН-группами при двойной связи — енолами.
Классификация и номенклатура. В зависимости от характера углеводородного радикала С могут быть ациклическими, или алифатическими (например, метиловый спирт, этиловый спирт, аллиловый спирт), алициклическими (циклогексанол), жирноароматическими (бензиловый спирт) и гетероциклическими. По числу ОН-групп в молекуле различают С одноатомные (алкоголи), двухатомные (гликоли),трехатомные (см. Глицерин), четырехатомные (см. Пентаэритрит) и др. многоатомные спирты (см. также Гекситы, Ксилит). ОН-группы в С могут быть связаны с первичным (—СН2ОН), вторичным (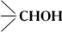 ) и третичным ( ) и третичным (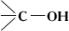 ) По этому признаку одноатомные С делят на первичные, вторичные и третичные. ) По этому признаку одноатомные С делят на первичные, вторичные и третичные.
Названия С обычно производят от названий соответствующих углеводородных радикалов: 3— (метиловый С), 25— (этиловый С), 37— (пропиловый С) и т.д. По Женевской номенклатуре к название соответствующего углеводорода прибавляют окончание "ол" (или диол, триол) и цифрой указывают номер с которым связана ОН-группа, например 3—()—3 (пропанол-2), 2-2—2 (пропандиол-1, 3). Иногда для построения название вторичных и третичных С употребляют т. н. рациональную номенклатуру (см. Номенклатура химическая). Некоторые С имеют тривиальные название, например этиловый С называется винным, метиловый С — древесным. С называются некоторые лекарственные средства, не имеющие отношения к этому классу соединений. Например, борный, камфорный и салициловый С представляют собой соответственно растворы борной кислоты, камфоры и салициловой кислоты в этиловом спирте, нашатырный С — водный раствор аммиака.
Свойства. Низшие одноатомные алифатические С — бесцветные жидкости, высшие (начиная с С12) — твердые вещества. С 1—3 обладают характерным алкогольным запахом и жгучим вкусом, 4—5 — сладковатым удушливым запахом (они придают неприятный запах сивушному маслу); высшие С без запаха. Простейшие гликоли и глицерины — вязкие жидкости. В жидком и твердом состоянии молекулы С связаны связями. Этим обусловлены их аномально высокие температуры кипения (например, 3 кипит при 64,7 °С, тогда как 3 — при 6 °С). С хорошо растворяются во многих органических растворителях и сами обладают хорошей растворяющей способностью. Неограниченно смешиваются с водой одноатомные С (1—3), гликоли (до 7), глицерин; растворимость в воде С (4—5) ограничена, высшие С нерастворимы. С образуют азеотропные смеси с водой и рядом органических соединений, что используется, например, при абсолютировании С
свойства С определяются наличием ОН-группы. При взаимодействии с щелочными и некоторыми др. металлами образуются солеобразные продукты — алкоголяты, например 25 (см. Алкоголяты и феноляты), с кислотами — эфиры сложные RCOOR" (см. также Этерификация); первичные С в мягких условиях окисляются в альдегиды RCHO и далее в карбоновые кислоты RCOOH, вторичные — в кетоны R——R. С сравнительно легко дегидратируются; при этом в зависимости от природы С и условий реакции образуются эфиры простые ROR или олефины. Взаимодействие с 5 и 2 приводит к алкилхлоридам RCl, RCl2 и т. д.
Получение и применение. В промышленности гидролизом алкилгалогенидов получают, например, амиловые спирты, бензиловый спирт; гидролиз сложных эфиров С и серной кислоты (алкилсульфатов) — важная стадия промышленного способа получения изопропилового спирта, этилового, трет-бутилового спиртов (см. Бутиловые спирты) из олефипов. Многие С синтезируют прямой гидратацией олефинов в присутствии катализаторов, восстановлением карбонильных соединений — альдегидов (получаемых, например, оксосинтезом, т. е. присоединением СО и 2 к олефинам) и кетонов, карбоновых кислот и их эфиров. Гидрогенизацией окиси получают, например, метиловый, н-пропиловый и изобутиловый С; этиловый и некоторые др. С — ферментативным брожением (см. Углеводы, Брожение, Гидролизная промышленность), некоторые высшие С — с помощью соединений (т. н. альфол-процесс).
С широко распространены в природе в свободном состоянии и в виде сложных эфиров. Например, жиры — эфиры глицерина (см. также Глицериды); воски —эфиры высших алифатических С; фенилэтиловый спирт и ментол — составные части соответственно розового и мятногоэфирных масел; цетиловый спирт найден в пчелином воске, эфир бензилового спирта и уксусной кислоты (бензилацетат) — в эфирном масле цветов жасмина.
С — важный в практическом отношении класс органических соединений; они служат полупродуктами в производстве красителей, синтетических волокон, пластических масс, лакокрасочных материалов, моющих средств, пластификаторов, эмульгаторов, лекарственных препаратов и т.д. С применяют как растворители, для приготовления алкилирующих агентов и др. Низшие алифатические С обладают слабым наркотическим действием, некоторые С ядовиты (например, метиловый спирт, этиленгликоль).
Лит.: Несмеянов А. Н., Несмеянов Н. А., Начала органической химии, т. 1—2, М., 1969—70.
В. Н. Фросин. |
Для поиска, наберите искомое слово (или его часть) в поле поиска
|

|
 |
 |
 |

|

|
Новости 10.06.2026 15:19:13
|

|

|
 |
|

|
 |
 |
 |
|