
|

|
Большая Советская Энциклопедия (цитаты)
|

|

|
 |
Ориентации правила | Ориентации правила (далее О) в органической химии определяют порядок замещения в ароматическом кольце при наличии в нем заместителя (ориентанта). При электрофильном ароматическом замещении (см. Замещения реакции, Нуклеофильные и электрофильные реагенты) ориентанты рода (, OR, OCOR, , SR, 2, NHR, NR2, алкилы, галогены) направляют замещение в орто- и пара-положения кольца, ориентанты рода (3, 2, , COOR, , 3, 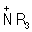 , ) - в мета-положение; при наличии ориентантов менее ярко выраженной природы (, RCO, 2, 22) наблюдается смешанная ориентация. Ориентирующий эффект обусловлен электронным влиянием заместителя на перераспределение электронной плотности в молекуле по системе простых (индуктивный -эффект) и сопряженных (мезомерный М-эффект) связей (см. также Мезомерия). Введение ориентантов рода увеличивает электронную плотность бензольного кольца в целом, но особенно в орто- и пара- положениях, введение ориентантов рода соответственно уменьшает. Ниже показано смещение электронной плотности в нитробензоле () и анилине (); дипольные моменты этих молекул 3,95 и 1,53Д соответственно: , ) - в мета-положение; при наличии ориентантов менее ярко выраженной природы (, RCO, 2, 22) наблюдается смешанная ориентация. Ориентирующий эффект обусловлен электронным влиянием заместителя на перераспределение электронной плотности в молекуле по системе простых (индуктивный -эффект) и сопряженных (мезомерный М-эффект) связей (см. также Мезомерия). Введение ориентантов рода увеличивает электронную плотность бензольного кольца в целом, но особенно в орто- и пара- положениях, введение ориентантов рода соответственно уменьшает. Ниже показано смещение электронной плотности в нитробензоле () и анилине (); дипольные моменты этих молекул 3,95 и 1,53Д соответственно:
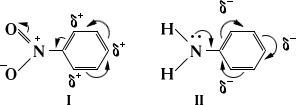
Еще более важно влияние ориентанта на распределение электронной плотности в переходном состоянии (см. Активированный комплекс). Предполагается, что структура переходного состояния близка к s-комплексу; она может быть изображена также набором резонансных структур (см. ниже). Ориентанты рода за счет индуктивного (+ или мезомерного (+M) эффектов (знаки + и - означают соответственно электронодонорный и электроноакцепторный характеры эффектов) облегчают электрофильное замещение, т.к. стабилизируют переходное состояние, частично погашая возникающий положительный заряд. Наиболее эффективно влияние ориентантов рода за счет сопряжения передается в орто- и пара-положения бензольного кольца, поэтому в эти положения в основном и направлена атака электрофила Е+. Примером может служить замещение в пара-положение толуола:
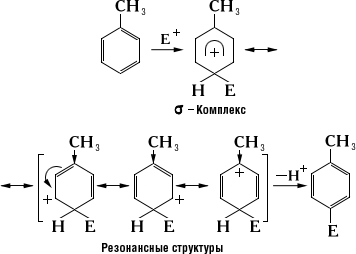
В возникающем переходном состоянии наблюдается прямое взаимодействие заместителя с положительным зарядом, в результате чего его энергия становится меньше, чем переходного состояния в случае мета-замещения в толуоле.
Более сложно поведение галогенных ориентантов, у которых -- и +М-эффекты действуют в противоположных направлениях. В нереагирующей молекуле из-за --эффекта галоген служит отрицательным концом диполя. В образующемся переходном состоянии при орто- и пара-замещении благодаря возможности частичного погашения заряда за счет +М-эффекта заместитель направляется именно в эти положения. Однако электрофильное замещение происходит труднее, чем в бензоле. Для заместителей, обладающих такой же комбинацией эффектов, например для аминогруппы (2), +М-эффект перекрывает действие --эффекта. Протонирование аминогруппы в растворах приводит к изменению характера ориентанта, т.к. 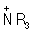 -группа пассивирует замещение и направляет его в мета-положение. -группа пассивирует замещение и направляет его в мета-положение.
Ориентанты рода за счет действия тех же эффектов в обратном направлении (-- и -М-эффекты) затрудняют вступление электрофила во все положения бензольного кольца, но особенно (за счет эффекта сопряжения) в орто- и пара-положения, поэтому в этом случае замещение в основном осуществляется в мета-положение, например как в нитробензоле:
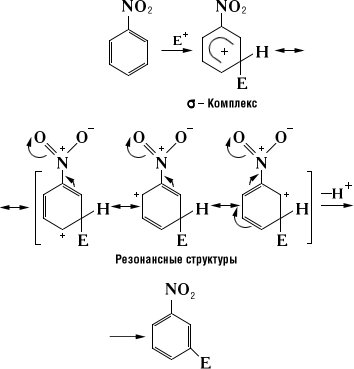
В возникающем переходном состоянии отсутствует прямое взаимодействие заместителя с положительным зарядом.
При наличии нескольких заместителей в ароматическом кольце возможны случаи согласованной и несогласованной ориентации, как, например, в n- и м-нитротолуолах. Относительная реакционная способность и эффект ориентации (избирательность реакции) в значительной степени зависят от характера электрофильного агента. Обратное влияние рассмотренных заместителей (как на активацию замещения, так и на ориентацию) наблюдается при нуклеофильном ароматическом замещении.
Лит.: Ингольд К., Теоретические основы органической химии, пер. с англ., М., 1973.
И. П. Белецкая.
|
Для поиска, наберите искомое слово (или его часть) в поле поиска
|

|
 |
 |
 |

|

|
Новости 10.06.2026 16:05:32
|

|

|
 |
|

|
 |
 |
 |
|