
|

|
Большая Советская Энциклопедия (цитаты)
|

|

|
 |
Ванадий | (далее В)(Vanadium), , элемент группы периодической системы номер 23, масса 50,942; металл серо-стального цвета. Природный В состоит из двух изотопов: 51 (99,75%) и 50 (0,25%); последний слабо радиоактивен (период полураспада Т1/2 = 1014 лет). В был открыт в 1801 мексиканским минералогом А. М. дель Рио в мексиканской бурой руде и назван по красивому красному цвету нагретых солей эритронием (от греч. erythrós — красный). В 1830 шведский химик Н. Г. Сефстрем обнаружил новый элемент в руде из Таберга (Швеция) и назвал его В в честь древнескандинавской богини красоты Английский химик Г. Роско в 1869 получил порошкообразный металлический В восстановлением 2 В промышленном масштабе В добывается с начала 20 в.
Содержание В в земной коре составляет 1,5-10-2% по массе, это довольно распространенный, но рассеянный в породах и минералах элемент. Из большого числа минералов В промышленное значение имеют патронит, роскоэлит, деклуазит, карнотит, и некоторые др. (см. Ванадиевые руды). Важным источником В служат и осадочные ( руды, а также окисленные руды. В извлекают как побочный продукт при переработке сырья, бокситов и различных органических отложений (асфальтиты, горючие сланцы). См. также Ванадаты природные.
Физические и свойства. В имеет объемноцентрированную кубическую решетку с периодом a = 3,0282 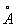 . В чистом состоянии В ковок, легко поддается обработке давлением. Плотность 6,11 г/см3, tпл 1900 ± 25°С, tкип 3400°С; удельная теплоемкость (при 20—100°С) 0,120 кал/гград; термический коэффициент линейного расширения (при 20—1000°С) 10,6·10-6 град-1, удельное электрическое сопротивление при 20 °С 24,8·10-8 ом·м (24,8·10-6 ом·см), ниже 4,5 К В переходит в состояние сверхпроводимости. Механические свойства В высокой чистоты после отжига: модуль упругости 135,25 н/м2(13520 кгс/мм2), предел прочности 120 нм/м2 (12 кгс/мм2), относительное удлинение 17%, твердость по Бринеллю 700 мн/м2 (70 кгс/мм2). Примеси газов резко снижают пластичность В повышают его твердость и хрупкость. . В чистом состоянии В ковок, легко поддается обработке давлением. Плотность 6,11 г/см3, tпл 1900 ± 25°С, tкип 3400°С; удельная теплоемкость (при 20—100°С) 0,120 кал/гград; термический коэффициент линейного расширения (при 20—1000°С) 10,6·10-6 град-1, удельное электрическое сопротивление при 20 °С 24,8·10-8 ом·м (24,8·10-6 ом·см), ниже 4,5 К В переходит в состояние сверхпроводимости. Механические свойства В высокой чистоты после отжига: модуль упругости 135,25 н/м2(13520 кгс/мм2), предел прочности 120 нм/м2 (12 кгс/мм2), относительное удлинение 17%, твердость по Бринеллю 700 мн/м2 (70 кгс/мм2). Примеси газов резко снижают пластичность В повышают его твердость и хрупкость.
При обычной температуре В не подвержен действию воздуха, морской воды и растворов щелочей; устойчив к неокисляющим кислотам, за исключением плавиковой. По коррозионной стойкости в соляной и серной кислотах В значительно превосходит и нержавеющую сталь. При нагревании на воздухе выше 300°С В поглощает и становится хрупким. При 600—700°С В интенсивно окисляется с образованием пятиокиси 25, а также и низших окислов. При нагревании В выше 700°С в токе образуется нитрид (tпл 2050°С), устойчивый в воде и кислотах. С В взаимодействует при высокой температуре, давая тугоплавкий карбид (tпл 2800°С), обладающий высокой твердостью.
В дает соединения, отвечающие валентностям 2, 3, 4 и 5; соответственно этому известны окислы: и 23 (имеющие основной характер), 2 (амфотерный) и 25 (кислотный). Соединения 2- и 3-валентного В неустойчивы и являются сильными восстановителями. Практическое значение имеют соединения высших валентностей. Склонность В к образованию соединений различной валентности используется в аналитической химии, а также обусловливает каталитические свойства 25. Пятиокись В растворяется в щелочах с образованием ванадатов.
Получение и применение. Для извлечения В применяют: непосредственное выщелачивание руды или рудного концентрата растворами кислот и щелочей; обжиг исходного сырья (часто с добавками ) с последующим выщелачиванием продукта обжига водой или разбавленными кислотами. Из растворов методом гидролиза (при рН = 1—3) выделяют гидратированную пятиокись В При плавке руд в домне В переходит в чугун, при переработке которого в сталь получают шлаки, содержащие 10—16% 25. шлаки подвергают обжигу с поваренной солью. Обожженный материал выщелачивают водой, а затем разбавленной серной кислотой. Из растворов выделяют 25. Последняя служит для выплавки феррованадия (сплавы с 35—70% В и получения металлического В и его соединений. Ковкий металлический В получают восстановлением чистой 25 или 23; восстановлением 25 вакуумным углетермическим восстановлением 23; восстановлением 13; термической диссоциацией В Плавят В в вакуумных дуговых печах с расходуемым электродом и в электроннолучевых печах.
Черная металлургия — основной потребитель В (до 95% всего производимого металла). В входит в состав быстрорежущей стали, ее заменителей, малолегированных инструментальных и некоторых конструкционных сталей. При введении 0,15—0,25% В резко повышаются прочность, вязкость, сопротивление усталости и износоустойчивость стали. В введенный в сталь, является одновременно раскисляющим и карбидообразующим элементом. Карбиды В распределяясь в виде дисперсных включений, препятствуют росту зерна при нагреве стали. В в сталь вводят в форме лигатурного сплава — феррованадия. Применяют В и для легирования чугуна. Новым потребителем В выступает быстро развивающаяся промышленность сплавов; некоторые сплавы содержат до 13% В В авиационной, ракетной и др. областях техники нашли применение сплавы на основе и содержащие присадки В Разрабатываются различные по составу жаропрочные и коррозионностойкие сплавы на основе В с добавлением , , , и , применение которых ожидается в авиационной, ракетной и технике. Интересны сверхпроводящие сплавы и соединения В с , и .
Чистый металлический В используют в энергетике (оболочки для тепловыделяющих элементов, трубы) и в производстве электронных приборов.
Соединения В применяют в промышленности как катализаторы, в сельском хозяйстве и медицине, в текстильной, лакокрасочной, резиновой, керамической, стекольной, фото и кинопромышленности.
Соединения В ядовиты. Отравление возможно при вдыхании пыли, содержащей соединения В Они вызывают раздражение дыхательных путей, легочные кровотечения, головокружения, нарушения деятельности сердца, почек и т.п.
В в организме. В — постоянная составная часть растительных и животных организмов. Источником В служат изверженные породы и сланцы (содержат около 0,013% В а также песчаники и известняки (около 0,002% В В почвах В около 0,01% (в основном в гумусе); в пресных и морских водах 1·107—2·107%. В наземных и водных растениях содержание В значительно выше (0,16—0,2%), чем в наземных и морских животных (1,5·10-5—2·10-4%). Концентраторами В являются: мшанка Plumatella, моллюск Pleurobranchus plumula, голотурия Stichopus mobii, некоторые асцидии, из плесеней — черный аспергилл, из грибов — поганка (Amanita muscaria). Биологическая роль В изучена на асцидиях, в кровяных клетках которых В находится в 3- и 4-валентном состоянии, то есть существует динамическое равновесие
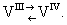
Физиологическая роль В у асцидии связана не с дыхательным переносом и углекислого газа, а с окислительно-восстановительными процессами — переносом электронов при помощи так называемой системы, вероятно имеющей физиологическое значение и у др. организмов.
Лит.: Меерсон Г. А., Зеликман А. Н., Металлургия редких металлов, М., 1955; Поляков А. Ю., Основы металлургии М., 1959; Ростокер У., Металлургия пер. с англ., М., 1959; Киффер ., Браун Х., пер. с нем., М., 1968; Справочник по редким металлам, (пер. с англ.), М., 1965, с. 98—121; Тугоплавкие материалы в машиностроении. Справочник, М., 1967, с. 47—55, 130—32; Ковальский В В Резаева Л. Т., Биологическая роль у асцидии, "Успехи современной биологии", 1965, т. 60, в. 1(4); Воwen Н. J. М., Trace elements in biochemistry, L. — . ., 1966.
И. Романьков. В В Ковальский. |
Для поиска, наберите искомое слово (или его часть) в поле поиска
|

|
 |
 |
 |

|

|
Новости 10.06.2026 17:25:59
|

|

|
 |
|

|
 |
 |
 |
|